お知らせ
タペンタ錠 薬価基準経過措置満了のご案内
日本緩和医療学会
会員各位
ムンディファーマ株式会社より、タペンタ錠の薬価基準経過措置期間が2025年3月31日をもって満了となった旨ご連絡がありましたので、会員の皆様にご案内申し上げます。
詳しくは、下記PDFをご確認ください。
持続性がん疼痛治療剤『タペンタ®錠25mg、50mg、100mg』薬価基準経過措置満了のご案内
日本緩和医療学会
理事長 木澤 義之
健康保険・介護保険委員長 石木 寛人
(2024年6月19日記事)
日本緩和医療学会
会員各位
タペンタ錠については、2024年2月20日付けの当学会ホームページでお知らせしましたとおり、疑義解釈委員会に製造並びに販売継続を望む要望書を提出し、厚生労働省など関係機関にもタペンタ錠の供給継続を依頼する働きかけを行ってまいりましたが、タペンタ錠の最終製造は既に終了しており、新たに製造を受託していただける企業が見つからないことから、これまで国内製造販売を担当してこられたムンディファーマ社およびヤンセンファーマ社が今後も国内販売を継続することが困難な状況です。
6月13日に開催しました理事会にて審議をおこないタペンタ錠の終売について当学会として承認することになりました。
今後のタペンタ錠の終売に向けてのスケジュールおよび質問に関しては、添付の案内状に記載されております、企業の問い合わせ先にお問い合わせください。
「医療関係者用」タペンタ錠_供給に関するお知らせとお願い_2024.06
日本緩和医療学会
理事長 木澤 義之
健康保険・介護保険委員長 石木 寛人
(2024年2月20日記事)
日本緩和医療学会
会員各位
ムンディファーマ株式会社よりタペンタ錠の販売停止案内状について、当学会のホームページへの掲載依頼があり、2月より採用施設においても販売停止に関するお知らせが届いていると聞いております。
医薬品の供給停止の手続きは下図のような順序で進められます。
供給停止にあたり、日本医師会疑義解釈委員会の審議結果を厚生労働省に報告する前に関係学会への検討依頼と了承又は供給継続要望を確認する手順となっております。
しかしながら、「タペンタ錠」に関して当学会からの要望を申し上げる機会はこれまでありませんでした。
現在、タペンタ錠の販売停止手続きは赤マーキングの段階となっています。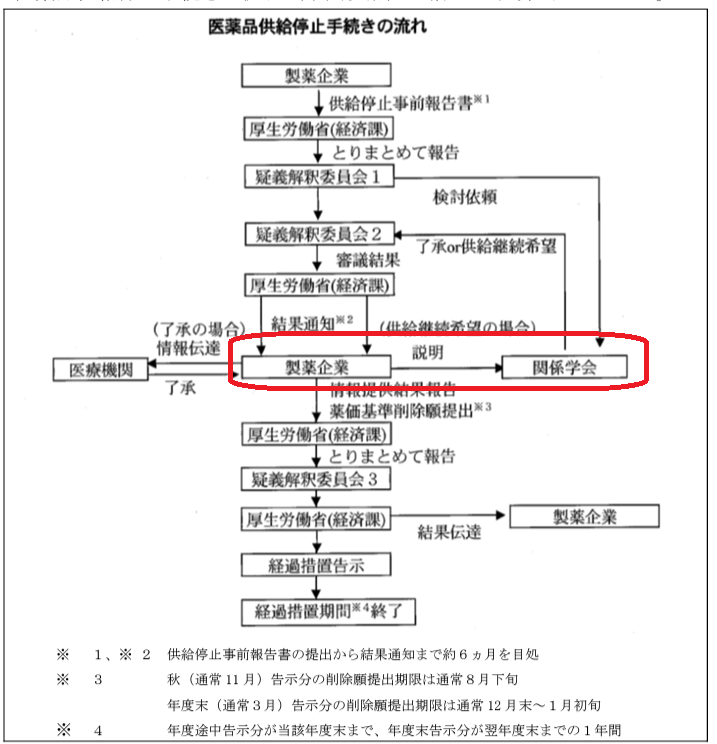
「タペンタ錠」は中等度から高度の疼痛を伴う各種癌における鎮痛の効能効果を有する薬剤であり、当学会より出版している「がん疼痛の薬物療法に関するガイドライン2020年版」においてタペンタドールは中等度から高度のがん疼痛に対して推奨度1B(強い推奨)とされています。
タペンタドール製剤は国内に代替品となる他社製品がなく、がん疼痛の治療領域では必須の医薬品となっております。
本品の供給が停止されるとがん疼痛治療に大きな支障をきたします。
従って、当学会では上記経緯を踏まえ、疑義解釈委員会に製造並びに販売継続を望む要望書を提出いたしました。
また、厚生労働省など関係機関にもタペンタドールの供給継続を依頼する働きかけを開始しております。
会員の皆様におかれましては、突然のニュースにご心配やご不安を抱いておられることと存じます。
患者様に不利益とならないよう、日本緩和医療学会として働きかけを行ってまいります。
日本緩和医療学会
理事長 木澤 義之
健康保険・介護保険委員長 石木 寛人